1. Généralités : étiologies, épidémiologie, sources d’exposition
Le terme amiante désigne un groupe de fibres minérales naturelles (silicate de magnésium hydraté), séparé en deux familles :
• Les serpentines, dont le seul représentant est le chrysotile. Ce dernier représente la variété commerciale de loin la plus importante (plus de 95% de l’amiante utilisée jusqu’à récemment).
• Les amphiboles, qui correspondent à la crocidolite l’amosite, l’anthophyllite, la trémolite et l’actinolite. Seules les deux premières variétés ont eu des utilisations commerciales importantes en France.
L’amiante a été utilisé dans l’industrie du fait de ses propriétés physiques et chimiques : ces fibres ont une grande résistance à la chaleur et ont donc été utilisées comme isolant thermique (flocage, cordelette, amiante tissé utilisé pour des gants, tabliers…, cartons). Il a une bonne résistance à divers produits chimiques. Enfin, il présente une résistance à la traction et à la friction. Il a été de ce fait utilisé comme matériau de renforcement dans les ciments (fibrociments), et dans la confection des garnitures de freins et embrayages.
Depuis le décret du 24 décembre 1996, la France a interdit la fabrication, la vente et l’importation de fibres d’amiante ou de produit en contenant, avec toutefois quelques exceptions (joints industriels, isolants thermiques industriels, garnitures de friction de véhicules lourds notamment).
Les affections consécutives à l’inhalation de poussières d’amiante sont les maladies respiratoires professionnelles qui font l’objet du plus grand nombre de réparations dans le régime général de la Sécurité sociale. Le nombre de cas repérés augmente régulièrement depuis une quinzaine d’années. Ce phénomène qui reflète l’augmentation de l’incidence des pathologies de l’amiante du fait de leur long temps de latence, est amplifié par un meilleur dépistage et des critères de reconnaissance moins restrictifs.
En 1999, 2273 cas ont fait l’objet d’une reconnaissance en maladie professionnelle dans le régime général de la Sécurité sociale : 1464 lésions pleurales bénignes (64,4% des cas), 218 asbestoses (19,6% des cas), 267 mésothéliomes (11,7% des cas) et 324 cancers bronchopulmonaires (14,3% des cas).
Les aspects épidémiologiques propres à chacune des pathologies de l’amiante seront évoqués dans le paragraphe diagnostic.
Les sources d’exposition professionnelle à l’amiante ont évolué dans le temps. Avant 1996, les principaux secteurs professionnels ayant conduit à des expositions à l’amiante concernaient les unités d’extraction, et les industries employant de l’amiante du fait de ses propriétés :
• Unités d’extraction (mines et moulins, afin de préparer des fibres de calibre donné)
• Fabrication de matériaux à base d’amiante : fabrication de fibro-ciment, de textile amiante, de matériaux de friction (freins, embrayages)
• Isolation (dans le bâtiment, dans la confection de fours industriels, dans la fabrication de matériel thermique et frigorifique, dans les chantiers navals) et calorifugeage (le flocage avec des produits contenant de l’amiante est interdit en France depuis 1977)
• Utilisation d’amiante comme protection contre la chaleur (gants, tabliers, cordons, couvertures…) dans diverses industries : chantiers navals, sidérurgie, fonderie, fabrication de verre, industrie du bâtiment…
Depuis l’interdiction de fabrication d’importation et de commercialisation de matériaux contenant de l’amiante en France (décret 96-1133 du 24/12/1996), c’est l’intervention sur des matériaux en place contenant de l’amiante qui constitue la préoccupation majeure, en particulier chez tous les professionnels du bâtiment.
Depuis quelques années une activité importante de retrait ou de confinement de l’amiante en place dans les bâtiments s’est également développée.
2. Les pathologies de l’amiante : diagnostic
Les pathologies de l’amiante, pleurales ou parenchymateuses pulmonaires, bénignes ou malignes, ont en commun plusieurs caractéristiques :
• Un temps de latence important : les maladies ne surviennent qu’exceptionnellement moins de 15 ans après le début de l’exposition
• Une persistance du risque toute la vie durant (le risque ne disparaît pas après arrêt de l’exposition)
• Un risque d’apparition corrélé à la dose cumulée d’amiante inhalé (relation dose-effet)
• L’absence fréquente de traitements curatifs.
2.1. La pathologie pleurale bénigne
Les lésions bénignes de la plèvre sont de loin les maladies liées à l’amiante les plus fréquentes.
2.1.1. LES PLAQUES PLEURALES
Les plaques pleurales sont des plages circonscrites de tissu conjonctif, riches en collagène, pauvres en cellules, recouvertes de cellules mésothéliales normales, développées au niveau de la plèvre pariétale. Elles siègent le plus souvent au niveau de la paroi thoracique antéro-latérale entre le troisième et le cinquième espace intercostal, au niveau de la paroi thoracique postérieure et latérale entre le cinquième et le huitième espace intercostal, et au niveau du dôme du diaphragme. Des plaques péricardiques sont également parfois observées.
Les plaques sont presque toujours asymptomatiques et de ce fait découvertes à l’occasion d’examens radiologiques systématiques, prescrits dans le cadre de la surveillance de sujets exposés ou ayant été exposés à l’amiante, ou à l’occasion d’affections respiratoires intercurrentes.
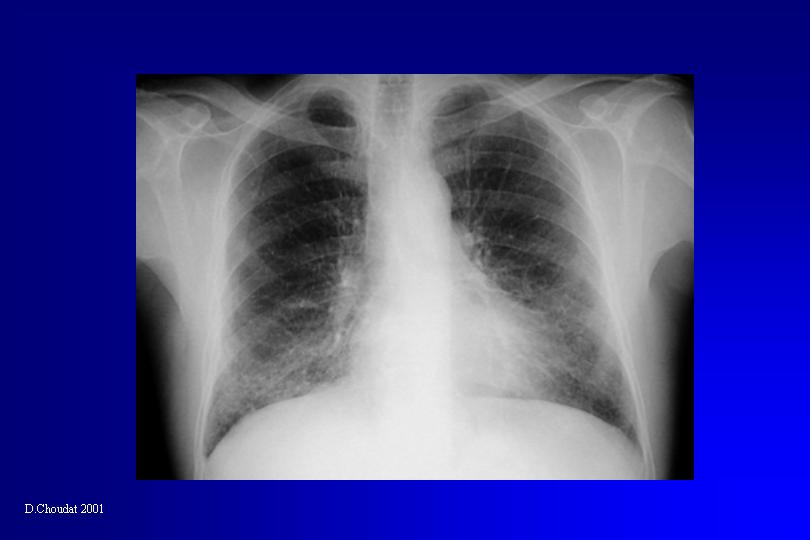
Sur une radiographie en incidence postéro-antérieure, elles apparaissent comme des opacités allongées, de contours nets, de densité hydrique, parallèles à la paroi latérale du thorax, ou comme des opacités paraissant se projeter en plein parenchyme pulmonaire, de contours irréguliers et de faible densité, sauf si elles sont calcifiées.
La tomodensitométrie permet de détecter des plaques plus fines et plus petites que la radiographie standard mais aussi de distinguer la fibrose pleurale de dépôts de graisse sous-pleurale ou d’insertions musculaires. En tomodensitométrie, les plaques sont caractérisées par des densités tissulaires, en surélévation le long de la face interne de la paroi thoracique, avec des angles de raccord abrupts, généralement multiples et bilatérales mais parfois unilatérales, plus ou moins calcifiées.
La prévalence des plaques pleurales est très importante dans les populations fortement exposées, pouvant dépasser 50 %. Des expositions environnementales faibles sont cependant suffisantes pour déterminer leur apparition.
Toutes les variétés minéralogiques d’amiante peuvent induire des plaques mais les amphiboles (crocidolite, amosite, trémolite, antophyllite) ont le plus fort pouvoir inducteur.
Le temps de latence est en général supérieur à 20 ans, et serait d’autant plus long que les expositions ont été plus faibles.
En l’absence de retentissement clinique et fonctionnel objectivable au niveau individuel, les plaques sont parfois considérées comme un marqueur d’exposition davantage que comme une réelle maladie. Néanmoins, plusieurs études récentes ont montré une réduction significative, quoique faible, des volumes pulmonaires, dans des groupes de sujets porteurs de plaques, comparativement à des sujets exposés mais indemnes de lésions pleurales, et ce même en l’absence de signes radiologiques de fibrose pulmonaire.
Le pronostic des plaques pleurales est excellent. Aucun traitement, aucun geste chirurgical à visée diagnostique ou thérapeutique, n’est justifié. A exposition identique à l’amiante, il n’existe actuellement aucune démonstration que les sujets porteurs de plaques ont un risque de CBP accru comparativement à des sujets sans plaques. Il en est de même pour le mésothéliome. Bien que le mésothéliome se développe initialement, commes les plaques, sur le feuillet pariétal de la plèvre, il n’est jamais le résultat de la transformation maligne d’une plaque.
2.1.2. LES ATTEINTES DE LA PLEVRE VISCERALE
2.1.2.1. La pleurésie asbestosique bénigne
La pleurésie asbestosique bénigne de l’amiante a été individualisée en 1964.
Faute d’anomalies histologiques spécifiques, son diagnostic repose sur la confirmation
d’une exposition à l’amiante et sur l’exclusion des autres causes de pleurésie, en particulier
le mésothéliome.
Les pleurésies bénignes de l’amiante sont habituellement peu abondantes, uni ou bilatérales, soit d’emblée, soit en cours d’évolution. Le liquide est un exsudat parfois sanglant, souvent riche en éosinophiles. Ces pleurésies sont spontanément résolutives et le diagnostic n’est souvent porté qu’à posteriori devant la constatation de séquelles pleurales à type de comblement du cul-de-sac costo-diaphragmatique. Le temps de latence de la pleurésie asbestosique bénigne est en moyenne de 30 ans mais quelques observations témoignent d’une apparition parfois précoce, inférieure à 10 ans, par rapport au début de l’exposition à l’amiante.
2.1.2.2. La fibrose de la plèvre viscérale
La fibrose de la plèvre viscérale doit être distinguée des plaques pleurales. Beaucoup moins fréquente que la fibrose de la plèvre pariétale, elle témoigne en effet de niveaux d’exposition en moyenne plus élevés que ceux qui sont responsables des plaques. De ce fait, elle est associée à un risque plus important de survenue de CBP ou de mésothéliome. De plus, son retentissement fonctionnel peut être important, contrairement à celui des plaques.
Souvent appelée épaississement pleural diffus, la fibrose de la plèvre viscérale est généralement séquellaire d’une pleurésie asbestosique bénigne, responsable d’une symphyse de deux feuillets pleuraux. Elle n’est pas spécifique d’une exposition à l’amiante. Tout épanchement pleural, quelle qu’en soit la cause – infectieuse, traumatique, inflammatoire, médicamenteuse – peut en effet entraîner une fibrose de la plèvre viscérale.
La fibrose de la plèvre viscérale, par son effet propre de « gangue » autour du poumon et par le retentissement parenchymateux qu’elle induit, entraîne un trouble ventilatoire restrictif parfois marqué, même en l’absence d’asbestose associée. La dyspnée d’effort et les douleurs thoraciques sont assez fréquentes.
Sur un cliché thoracique de face, la fibrose de la plèvre viscérale est caractérisée par un épaississement plus ou moins étendu en hauteur, à bords souvent irréguliers, associé à un comblement du sinus costo-diaphragmatique homolatéral.
En tomodensitométrie la différence avec une plaque pleurale repose partiellement sur des critères dimensionnels (étendue et épaisseur plus grandes en général) mais surtout sur l’existence de signes témoignant d’un retentissement parenchymateux en regard de l’épaississement. Ce retentissement peut prendre l’aspect de bandes parenchymateuses ou d’atélectasies par enroulement :
• les bandes parenchymateuses sont des hyperdensités, longues de 2 à 5 cm, larges de quelques millimètres, partant de la plèvre et barrant le parenchyme pulmonaire ;
• les atélectasies par enroulement sont caractérisées par une masse arrondie de quelques centimètres de diamètre, située à la périphérie du poumon, adossée à la surface pleurale, avec un angle de raccordement aigu entre la plèvre et l’opacité, une diminution du volume pulmonaire homolatéral et un aspect en queue de comète constitué par les vaisseaux et les bronches qui pénètrent dans l’atélectasie en s’enroulant. Lorsque tous les critères radiologiques sont réunis il est inutile de procéder à des gestes à visée diagnostique invasifs.
Atelectasie ronde au scanner
La localisation préférentielle des atélectasies par enroulement au niveau des lobes inférieurs, en position latéro-vertébrale, fait qu’elles sont rarement visibles sur une radiographie thoracique de face, car elles sont masquées par l’ombre cardiaque.
2.2. L’asbestose
Le terme asbestose, souvent improprement utilisé pour désigner l’ensemble des pathologies asbestosiques bénignes, doit être réservé à la fibrose interstitielle pulmonaire induite par l’inhalation d’amiante.
Les niveaux d’exposition nécessaires pour provoquer une asbestose sont importants. Il s’agit donc d’une pathologie rare comparativement à la pathologie pleurale asbestosique bénigne. On peut en espérer la disparition progressive compte-tenu de la suppression des industries de transformation de l’amiante et de l’amélioration progressive des conditions de travail, dans les secteurs d’activité où les personnels sont encore amenés à intervenir sur des matériaux contenant de l’amiante.
La fibrose asbestosique, initialement localisée au niveau des bifurcations bronchiques périphériques, peut s’étendre progressivement à l’ensemble de l’interstitium pulmonaire. Il s’agit d’une maladie cliniquement et radiologiquement proche de la fibrose pulmonaire idiopathique. Son diagnostic repose sur la confrontation des signes radiologiques avec l’anamnèse professionnelle.
Les signes radiographiques de l’asbestose sont des petites opacités irrégulières (réticulées), généralement bilatérales et symétriques prédominant dans les régions basales et sous-pleurales. Dans les formes débutantes ces images sont difficiles à distinguer de la trame vasculaire normale. Les images en rayon de miel s’observent dans les formes avancées. La radiographie thoracique est souvent prise en défaut. Environ 15 % des asbestoses diagnostiquées par la tomodensitométrie thoracique sont inapparentes sur un cliché thoracique standard. A l’inverse, la radiographie thoracique expose à un risque important de faux positifs, en particulier ches les fumeurs et les obèses.
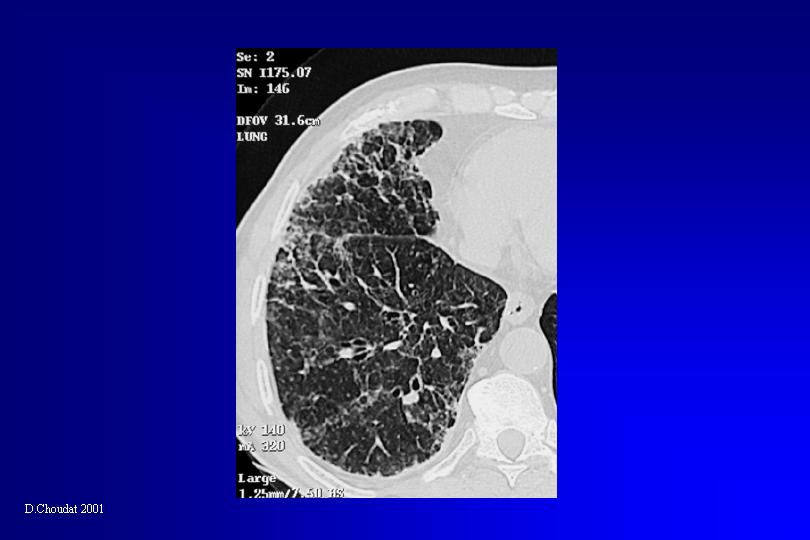
La tomodensitométrie en haute-résolution est devenue sans contexte l’examen de choix. La sémiologie tomodensitométrique comprend :
– les lignes septales, opacités linéaires de 1 à 2 cm de longueur, prédominant dans les régions postérieures et inférieures ;
– les lignes non septales, plus courtes, radiaires au départ de l’artère centrolobulaire, correspondant à la fibrose péribronchiolaire ;
– les lignes courbes sous-pleurales, hyperdensités curvilignes situées à proximité de la plèvre et parallèles à la paroi thoracique ;
– le rayon de miel caractérisé par des cavités kystiques de quelques millimètres de diamètre, aux parois épaisses.
Ces images élémentaires peuvent être diversement associées d’un patient à l’autre et doivent être recherchées en procubitus pour s’affranchir du problème des opacités déclives. La signification des opacités en verre dépoli est encore débattue en raison de leur très faible spécificité.
Les anomalies cliniques sont en général peu précoces, retardées par rapport aux signes radiologiques. Les symptômes sont la dyspnée d’effort et la toux. Des râles crépitants inspiratoires aux deux bases sont fréquemment audibles et ce de façon parfois très précoce. L’hippocratisme digital est inconstant. Certaines asbestoses sont très peu évolutives, d’autres sont susceptibles d’évoluer progressivement vers une insuffisance respiratoire sévère. Les facteurs associés à une évolution péjorative sont la durée de l’exposition à l’amiante et l’intensité de cette exposition.
Une cause de mortalité fréquente des patients porteurs d’une asbestose est le CBP. La nature des relations entre l’asbestose et le CBP demeure controversée. Deux théories s’affrontent. Selon la première, il existerait une relation causale entre l’asbestose et le CBP. Selon le deuxième il s’agirait de deux maladies indépendantes admettant l’amiante comme étiologie commune.
Les données épidémiologiques recueillies au cours des dernières années militent plutôt en faveur de la seconde théorie. Un excès de risque de CBP a en effet été observé dans des populations de sujets exposés à l’amiante mais indemnes de signes radiographiques d’asbestose.
A exposition identique à l’amiante, il semble néanmoins que l’existence d’une asbestose confère un risque de CBP majoré par rapport à l’exposition seule.
2.3. Le cancer broncho-pulmonaire
Il n’existe pas de signes cliniques, radiologiques ou histopathologiques permettant de rattacher avec certitude un CBP à une exposition professionnelle à l’amiante. Depuis 1955 de nombreuses études de cohorte ont démontré sans équivoque que la mortalité par CBP est plus élevée parmi les travailleurs exposés à l’amiante que parmi la population générale. Il est actuellement admis que l’amiante représente le principal facteur étiologique professionnel des CBP. En France le nombre de décès par CBP attribuables à une exposition à l’amiante a été estimé à 1200 cas pour l’année 1996 par le groupe d’expertise collective mis en place par l’INSERM. Le risque de CBP croît de façon linéaire avec l’augmentation de l’exposition cumulée à l’amiante. L’existence d’un excès de risque de CBP pour les niveaux d’exposition faibles ou modérés reste controversé. Des études environnementales n’ont pas mis en évidence d’excès de risque mesurable de décès par CBP chez des femmes résidant à proximité des mines de chrysotile du Québec. L’épidémiologie ne peut pas apporter des réponses à cette interrogation car il faudrait pouvoir suivre de façon prolongée des cohortes de plusieurs dizaines de milliers de personnes.
L’interaction amiante-tabac dans l’induction de cas de CBP a fait l’objet de plusieurs études qui témoignent d’un modèle approximativement multiplicatif. A exposition identique à l’amiante, le nombre de cas de CBP attribuables à une exposition à l’amiante est donc plus important dans une population de fumeurs que dans une population de non-fumeurs. Néanmoins, la probabilité qu’un CBP soit provoqué par une exposition à l’amiante est indépendante de la consommation de tabac. Elle dépend uniquement de l’intensité et de la durée de cette exposition.
Tous les types histologiques peuvent être observés. Une surreprésentation des adénocarcinomes est inconstamment retrouvée. Toutes les variétés minéralogiques de fibres d’amiante – chrysotile et amphiboles – peuvent être à l’origine de CBP. L’analyse minéralogique d’échantillons biologiques – liquide de lavage broncho-alvéolaire ou biopsie pulmonaire – permet, par la quantification en microscopie optique des corps asbestosiques (CA), d’évaluer la rétention pulmonaire et d’évaluer ainsi l’exposition cumulée à l’amiante en complément des données de l’interrogatoire professionnel, parfois difficile à mener et souvent pris en défaut pour les expositions anciennes. Une exposition significative à l’amiante est probable lorsque la concentration est supérieure à 1 CA/ml dans le liquide de lavage broncho-alvéolaire, ou supérieur à 1000 CA/g de tissu sec dans le poumon.
2.4. Le mésothéliome
Le mésothéliome est une tumeur maligne qui affecte prioritairement le plèvre, plus rarement le péritoine, beaucoup plus rarement encore le péricarde ou la vaginale testiculaire. Il s’agit d’une tumeur très rare dans les populations non exposées à l’amiante. Son incidence « spontanée » est évaluée à 1 ou 2 cas annuels par million d’habitants. L’augmentation importante de l’incidence du mésothéliome observée dans les populations masculines depuis les années cinquante est en rapport avec l’utilisation croissante de l’amiante. Une exposition l’amiante est retrouvée chez 60 à 80 % des patients atteints de mésothéliome. L’incidence annuelle du mésothéliome varie de 1 à 10/million chez la femme et de 2 à 50/million chez l’homme dans les pays industrialisés. Pour la France les chiffres étaient en 1992 de 9,2/million chez la femme et 22,5/million chez l’homme. En 1996, le nombre de décès par mésothéliome attribuables à l’amiante a été évalué à 750. Compte tenu du temps de latence très long de cette tumeur, 35 à 40 ans en moyenne, les effets des dispositions réglementaires concernant la prévention primaire, prises à partir de 1977, ne se feront probablement pas sentir avant de nombreuses années. Les modèles prédictifs élaborés pour la France permettent de prévoir un pic de mortalité par mésothéliome autour de 2020. Environ 20 000 décès devraient survenir chez l’homme et 2900 chez la femme, entre 1996 et 2020.
Le risque de la maladie augmente en fonction de la dose cumulée d’exposition et du temps écoulé par rapport au début de l’exposition. Contrairement aux CBP, il est établi que des excès significatifs de mésothéliome sont détectables, même pour des expositions cumulées à l’amiante très faibles. Par ailleurs, il existe un gradient de cancérogénicité pleurale en fonction du type de fibres inhalées. Les fibres d’amphiboles, en particulier de crocidolite, sont beaucoup plus mésothéliogènes que les fibres de chrysotile.
Le rôle du virus SV 40, qui dans les années 60 contaminait les vaccins anti-poliomyélitiques, a été récemment évoqué comme co-facteur de l’amiante, en raison de la découverte de fragments du génome de ce virus dans les cellules mésothéliomateuses de nombreux malades. Il existe en revanche un consensus pour considérer que le rôle du tabagisme est nul.
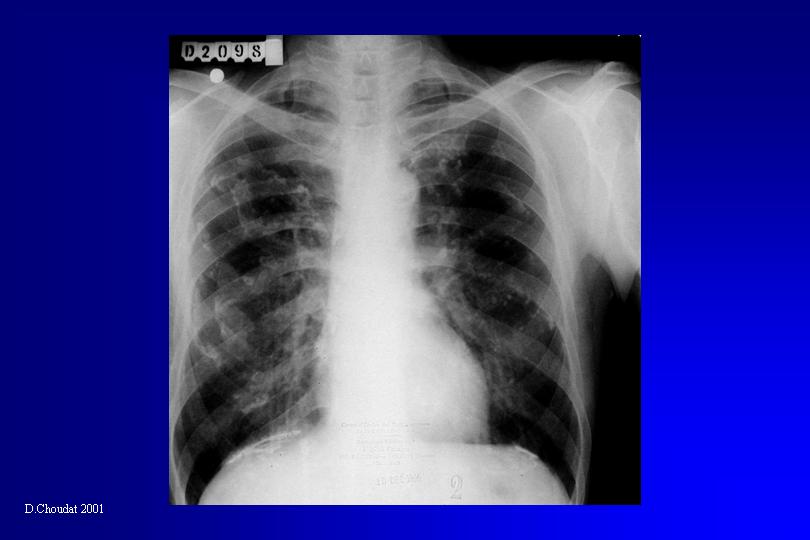
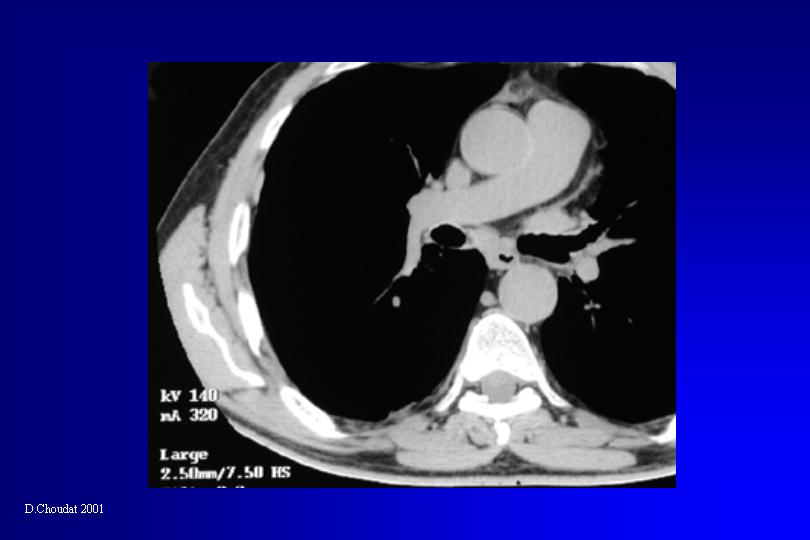
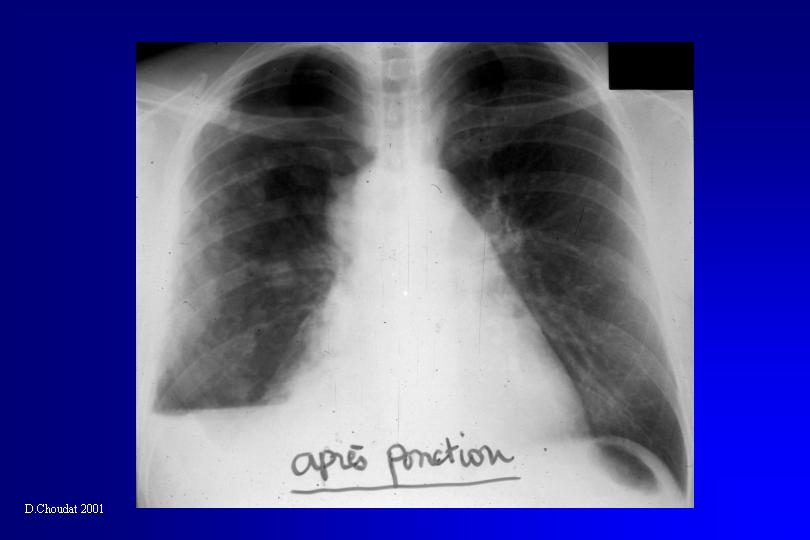
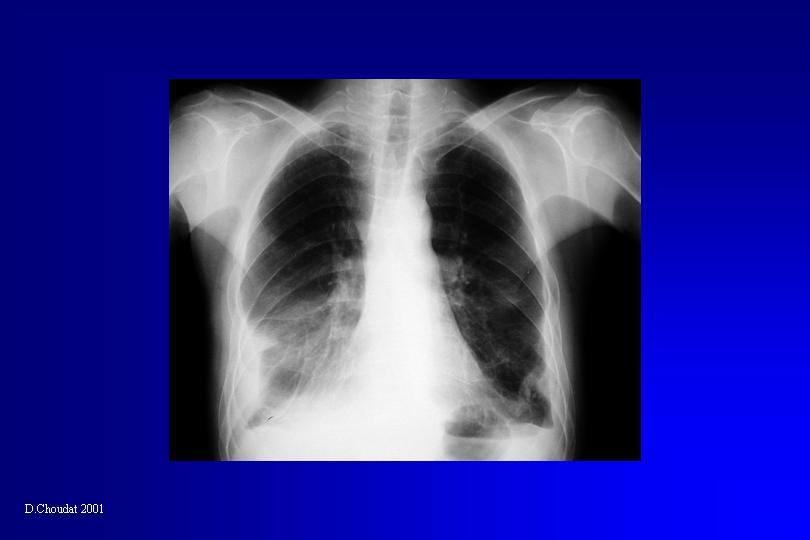
Les manifestations cliniques du mésothéliome les plus fréquentes sont les douleurs thoraciques, la dyspnée et l’altération de l’état général. Un épanchement pleural est présent dans 80 à 90 % des cas, révélé par la radiographie thoracique. L’aspect de plèvre épaissie et festonnée est évocateur mais tardif. En tomodensitométrie les formes évoluées sont caractérisées par un épaississement circonférenciel irrégulier, mamelonné, de la plèvre pariétale, associé à une rétraction de l’hémithorax. La thoracoscopie représente la technique diagnostique de choix. Elle permet la réalisation de biopsies pleurales multiples avec un rendement de 95 %, bien supérieur à celui de la cytologie pleurale ou de la biopsie transpariétale. Le diagnostic histologique est difficile. L’immunohistochimie apporte une aide considérable, grâce à l’utilisation d’anticorps monoclonaux, marqueurs positifs ou négatifs de la cellule mésothéliale.
En l’absence de traitement standardisé ayant fait la preuve de son efficacité, le pronostic du mésothéliome, quelle qu’en soit la localisation, demeure actuellement très sombre, avec une survie médiane de 7 à 15 mois et un taux de survie à 5 ans inférieur à 5 %.
2.5. Autres cancers
Un lien possible avec une exposition à l’amiante a été évoqué pour plusieurs sites extra-respiratoires de cancers.
Le cancer du larynx est le site pour lequel le lien avec l’exposition à l’amiante est le plus suspecté. En effet un excès significatif de risque de cancer du larynx a été observé dans plusieurs études de cohorte ou études cas-témoin. Néanmoins la prise en compte souvent absente ou insuffisante des facteurs de confusion que sont la consommation d’alcool et de tabac ne permet pas actuellement de conclure avec certitude à l’existence d’un lien de causalité.
Il existe également quelques données épidémiologiques en faveur d’un lien de causalité entre exposition à l’amiante et cancers digestifs ou uro-génitaux. En l’absence de relation dose-effet clairement démontrée, il apparaît prématuré de conclure actuellement.
3. Prévention
La prévention s’appuie sur une réglementation spécifique, notamment :
• Arrêté du 11/07/1977 pour la mise en surveillance médicale spéciale des salariés exposés au risque amiante
• Décret 96-97 du 7/02/1996 relatif à la protection de la population contre les risques sanitaires liés à une exposition à l’amiante dans les immeubles bâtis
• Décret 96-98 du 7/02/1996 relatif à la protection des travailleurs exposés au risque amiante et les arrêtés et circulaires d’application qui en découlent.
L’arrêté du 13/12/1996 précise les moyens à mettre en œuvre par le médecin du travail pour la surveillance des salariés exposés à l’amiante :
• Evaluation du risque
• Information en formation des salariés exposés
• Conseil en terme de protection individuelle
• Appréciation du risque par la visite des lieux de travail
• Modalités de la surveillance médicale pendant son activité professionnelle et après l’exposition.
Les grandes lignes des actions préventives sont :
• Protections collectives (confinement de la zone où un opérateur intervient sur de l’amiante)
• Protections individuelles (port de masque à poussières type P3 lors des opérations ponctuelles ou de cagoule à adduction d’air pour des opérations plus lourdes)
• Il est important d’obtenir des patients un arrêt de leur tabagisme, du fait de la synergie amiante-tabac pour le risque de cancer bronchopulmonaire
• Respect de la valeur limite d’exposition en milieu de travail (0,1 f/cm3 sur 1 heure de travail en 1997)
• Une surveillance radiologique et fonctionnelle respiratoire est proposée en milieu de travail pour dépister les formes débutantes chez les salariés ayant été ou pouvant encore être exposés. Cette surveillance est prolongée après cessation de l’activité (suivi post-professionnel).
4. Réparation
Les tableaux 30 et 30 bis du régime général de la Sécurité sociale et le tableau 47 du régime agricole permettent, sous certaines conditions, l’indemnisation des pathologies de l’amiante.
Des modifications récentes permettent d’indemniser les plaques pleurales mêmes unilatérales.
Les CBP peuvent être indemnisées, quelle que soit la durée d’exposition, lorsqu’ils sont associés à des pathologies asbestosiques bénignes, pleurales ou parenchymateuses. En l’absence de lésions bénignes, une durée minimum d’exposition au risque de 10 ans est nécessaire, ainsi que l’exercice d’un emploi mentionné dans une liste limitative. Si ces critères ne sont pas remplis une reconnaissance peut néanmoins être obtenue après examen du dossier par un Comité régional de reconnaissance des maladies professionnelles (CRRMP).
Des dispositions réglementaires récentes permettent aux patients ayant une maladie liée à l’amiante reconnue en maladie professionnelle de bénéficier d’une cessation anticipée d’activité à partir de l’âge de 50 ans. Le dispositif d’allocation de cessation anticipée d’activité est également ouvert, en l’absence de maladie professionnelle, aux anciens salariés des établissements de fabrication de matériaux contenant de l’amiante et de certains établissements utilisateurs comme les entreprises d’isolation. Peuvent également bénéficier de ce dispositif les salariés des entreprises de flocage et calorifugeage et sous certaines conditions les dockers et salariés du secteur de la construction et réparation navale.
Outre le système classique de réparation entrant dans le cadre des tableaux de maladie professionnelle, la loi n° 2000-1257 du 23 décembre 2000 de financement de la Sécurité sociale pour 2001 prévoit la création d’un Fonds d’indemnisation des victimes de l’amiante (FIVA).
Le FIVA, financé par l’Etat et les employeurs, a pour principe la réparation intégrale de tous les préjudices subis (préjudice fonctionnel, préjudice professionnel, préjudice moral…) et concerne toutes les victimes de l’amiante, quelle que soit l’origine de la maladie (professionnelle ou environnementale) et quel que soit le statut de la personne (salariés, fonctionnaires, artisans, sans emploi…).